Tangerang Selatan, Humas BRIN. Hanggara Sudrajat, periset Pusat Riset Fisika Kuantum – Badan Riset dan Inovasi Nasional (BRIN), pada Selasa (17/5) menceritakan penelitiannya yang berjudul ‘Perangkat Fotokatalitik untuk Konversi Energi dan Transformasi Kimia’. Topik riset tersebut dipresentasikan pada webinar ornamat seri #2 tahun 2022 di lingkungan Organisasi Riset Nano Teknologi dan Material BRIN.
Hanggara mempresentasikan satu contoh fotokatalis yaitu karbon nitrida (CN) ermuat tembaga oksida, yaitu Cu(I)Ox-C3N4, yang digunakan pada fotoreaktor mikrofluidik.
Pemanenan Energi Surya
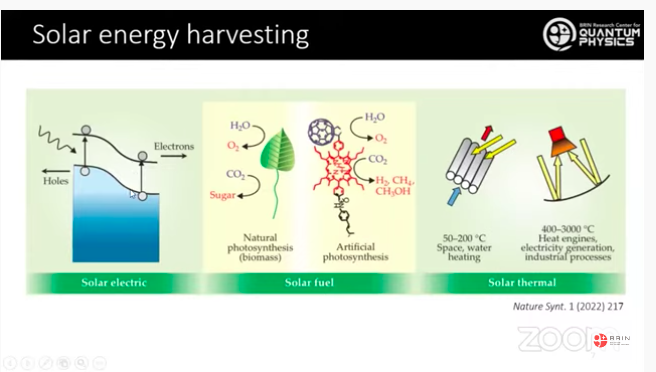
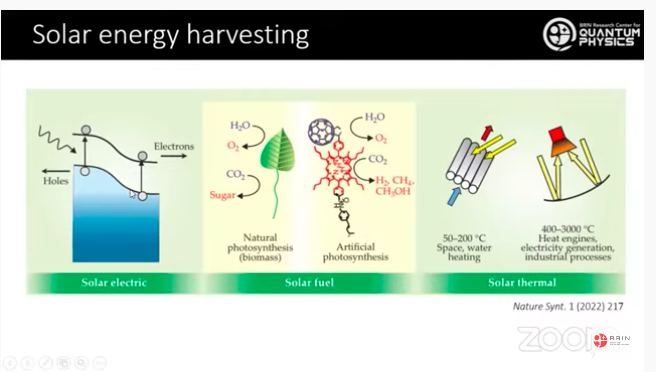
Pemanenan energi surya (solar energy harvesting) memiliki tiga rute utama, yaitu solar electric, solar fuel, dan solar thermal. Topik yang ditekuni Hanggara dan tim yaitu solar fuel atau bahan bakar surya.
Bahan bakar surya prinsipnya meniru apa yang dilakukan tumbuhan hijau pada fotosintesis alami. “Kami meniru apa yang dilakukan tumbuhan hijau dengan harapan dapat mendapatkan efisiensi yang jauh lebih tinggi. Tumbuhan hijau itu kebanyakan hanya bisa menggunakan cahaya di daerah merah, makanya berwarna hijau. Daerah lain pada cahaya tampak belum termanfaatkan oleh tumbuhan” terang Hanggara.
Fotosintesis Artifisial
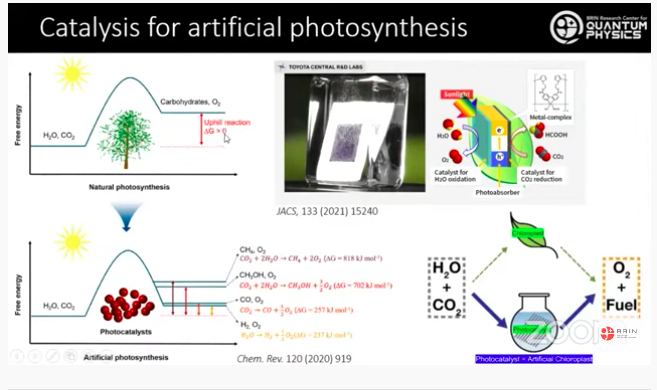
Pada fotosintesis alami, tumbuhan hijau mengonversi molekul-molekul berenergi rendah, misalnya karbon dioksida , dan air, menjadi molekul yang berenergi tinggi, misalnya sukrosa, dengan tujuan menyimpan energi dari matahari dalam bentuk ikatan kimia.
“Kita tiru bagaimana kloroplas bekerja pada tumbuhan hijau, dan menggantinya secara artifisial dengan sebuah entitas kimia yang kita sebut sebagai katalis. Karena katalisnya ini bekerja berdasarkan pada penyerapan foton, maka kita sebut saja sebagai fotokatalis. Fotokatalis ini sistemnya bisa homogen maupun heterogen, dan bisa berupa, molekul organik maupun anorganik. Itu bergantung dari opsi kita yang harus disesuaikan dengan target reaksinya dan produk fotokimia seperti apa yang diinginkan,” urai Hanggara.
Biasanya untuk molekul-molekul organik seperti senyawa-senyawa kompleks logam transisi, selektivitasnya tinggi, tetapi kurang stabil. Sedangkan material anorganik seperti oksida logam selektifitasnya rendah namun stabil.
Pada penelitiannya, fotokatalis lebih kerap digunakan, karena relatif mudah sintesisnya dan murah prekursornya.
“Karena pada prinsipnya kloroplas pada tumbuhan hijau kita tiru (mimicking) prosesnya secara artifisial menggunakan fotokatalis, maka fotokatalis ini kerap disebut sebagai kloroplas artifisial,” kata Hanggara.
Prinsip Kerja Fotokatalis
Prinsip kerja fotokatalis adalah pemanfaatan eksiton, yaitu elektron dan lubang elektron (hole) yang diproduksi oleh katalis ketika menyerap foton, untuk menjalankan berbagai reaksi fotokimia, misalnya a) pemisahan air (water splitting) untuk menghasilkan bahan bakar hidrogen, b) degradasi polutan dan c) konversi karbon dioksida (CO2) menjadi bentuk-bentuk karbon dioksida tereduksi.
“Jadi pada intinya fotokatalis menyerap partikel cahaya atau foton kemudian digunakan untuk mengeksitasi elekctron dan meninggalkan lubang elektron, sehingga elektron dan lubang elektron bisa kita manfaatkan untuk menjalankan berbagai reaksi fotokimia, “ jelasnya.
Ketika elektron dan lubang elektron terproduksi, mereka berpindah ke permukaan partikel katalis secara acak karena tidak ada bias eksternal yang ditambahkan seperti pada perangkat fotovoltaik. Sehingga elektron dan lubang elektron harus diarahkan dan tidak bertemu kembali (ekombinasi).
Elektron dan lubang elektron diarahkan ke permukaan katalis oleh katalis lain sehingga kita sebut sebagai ko-katalis.
“Ko-katalis ini sangat penting karena menentukan kuantum efisiensi secara keseluruhan. Di bidang fotokatalisis, banyak orang berusaha dengan beragam cara untuk mengembangkan ko-katalis yang mampu untuk mengekstrak elektron dan lubang elektron secara efisien,” ungkap Hanggara.
Perangkat Fotokatalitik
Contoh perangkat fotokatalitik juga mengikuti perkembangan material fotokatalisnya. Misalnya untuk Solar water splitting ada berbagai opsi seperti sistem fotovoltaik, elektrolisis, fotoelektrokimia, dan fotokatalisis
“Fokus riset kami adalah fotokatalis yaitu sistem yang katalisnya berupa partikel atau serbuk (powdered photocatalyst), dan lapis tipis (photocatalyst sheets). Sistem ini sangat sederhana karena tidak memerlukan bias eksternal. Tinggal memasukkan saja serbuk fotokatalisnya ke dalam air kemudian disinari dengam lampu xenon atau sinar matahari langsung, maka akan segera timbul gelembung-gelembung gas hidrogen dan oksigen,” urai Hanggara.
Cu(I)Ox-C3N4 untuk Fotorekator Mikrofluidik
Kembali ke Cu(I)Ox-C3N4. Hanggara dan tim mengambil satu contoh fotokalis yaitu karbon nitrida ermuat tembaga oksida.
Karbon nitrida adalah polimer organik yang dapat disintesis dari prekursor apa saja yang mengandung nitrogen dan karbon sebagai unsur utamanya, misalnya urea. “Beberapa keunggulan karbon nitrida adalah murah, sangat mudah dipreparasi, komposisi, dan morfologi bisa diatur dengan sangat fleksibel, fotostabil, tidak beracun, dan mudah didapatkan bahan bakunya,” terangnya.
“Komposisi juga bisa kita desain sedemikian rupa, sehingga kita bisa mendapatkan berbagai macam variasi karbon nitrida (CN) dengan struktur dan morfologi yang berbeda dan tentu juga foto aktivitasnya akan menjadi berbeda. Makanya kita bisa mengatur sesuai target reaksinya,” tambahnya.
Sebagai satu contoh misalnya karbon nitrida yang termuat tembaga (I) oksida atau Cu (I) dengan konsentrasi sekitar 8%. Preparasi ini sangat mudah, misalnya pakai urea sebagai prekursornya. Kemudian tinggal dipanaskan saja pada suhu 550 °0C atau suhu berapun di atas 400 °C, untuk mendapatkan berbagai macam struktur, komposisi, dan morfologi yang berbeda. Seperti pada penelitian ini, bisa ditambahkan tembaga untuk meningkatkan fotoaktivitas dari Cu(I)Ox-C3N4.
“Jika kita lihat, ini murah proses produksinya dan mudah didapatkan prekursornya. Dua faktor ini sangat penting untuk langkah selanjutnya, karena murah dan bagus, itu menjadi kunci untuk aplikasi di industri,” ucapnya.
“Kalau tidak murah dan tidak bagus, maka orang tidak bisa menjual, sehingga ketika hasil penelitian ke luar dari lab, dia tidak bisa berlanjut ke industri. Jadi prinsipnya harus semurah mungkin dan sebagus mungkin,” tegas Hanggara.
Struktur Elektronik
Kemudian setelah dideposisi dengan tembaga, kita ingin tahu sebenarnya, apa fungsi tembaga? “Seperti yang saya ungkapkan tadi, tembaga ini cukup murah, jadi jika ternyata bisa meningkatkan performa secara signifikan tentu ini merupakan berita bagus karena bisa menggantikan fungsi logam mulia yang selama ini digunakan sebagai ko-katalis seperti misalnya Pt, Ru, Rh dan Re,” kata Hanggara.
Dengan spektroskopi fotoelektron ultraviolet ternyata diketahui bahwa posisi atau potensial dari pita valensinya (VB) cukup rendah (relatif positif), sehingga bisa mendorong berbagai macam reaksi oksidasi untuk keperluan transformasi kimia.
Kemudian dilihat dengan hard-XAS, ternyata tembaga ini ada dalam bentuk embaga bervalensi satu atau Cu(I) oksida, mirip dengan Cu2O.
Selanjutnya, soft-XAS, mengindikasikan bahwa spesies tembaga oksida ini lebih dominan berinteraksi dengan nitrogen, dibandingkan dengan karbon pada karbon nitrida host-nya, karena nitrogen memiliki 6 pasangan elektron bebas
Mekanisme Fotoaktivasi
Jadi setelah dievaluasi untuk menghasilkan hidrogen melalui reaksi reduksi proton menghasilkan hidrogen, ternyata tembaga dapat meningkatkan laju reaksinya beberapa kali.
“Tentu kita ingin tahu kenapa seperti itu, ternyata setelah melalui tahap karakterisasi dengan berbagai teknik karakterisasi lanjut, diketahui bahwa populasi elektron meningkat namun mobilitas elektronnya menurun. Uniknya, waktu hidup (lifetime) dari elektronnya makin lama,” papar Hanggara.
Karakterisasi lebih lanjut dengan spektroskopi fotoakustik menunjukan bahwa populasi perangkap elektron (electron trap) pada karbon nitrida lebih besar setelah termuat tembaga oksida. “Jadi ini menjawab kenapa elektron populasi lebih tinggi namun mobilitas elektron lebih rendah, dan efeknya adalah waktu hidup elektron lebih lama. Hal ini dikarenakan elektron terperangkap oleh spesies tembaga oksida,” lafalnya.
Waktu hidup elektron yang lebih lama akan menaikan probabilitas elektron untuk bereaksi dengan proton menghasilkan hidrogen,” imbuhnya.
Perangkat Berbasis Mikrofluidik
Hanggara dan tim kemudian mengaplikasikan fotokatalis pada reaktor mikrofluidik untuk menjalankan suatu reaksi fotokimia.
Fotokatalisis Cu(I)Ox-C3N4 pada reaktor mikofluidik berpotensi mewujudkan konsep kimia hijau untuk transformasi kimia yang relevan secara industri. Fotokatalis ini murah produksinya dan memiliki selektivitas tinggi.
Dari riset ini dapat diketahui bahwa Cu(I) spesies ini dapat digunakan sebagai ko-katalis, untuk meningkatkan performa karbon nitrida, dengan cara meningkatkan waktu hidup elektron melalui proses electron trapping pada perangkap dangkal (shallow trap), sehingga potensial .sebagai pengganti logam mulia seperti Pt, Rh, Ru, dan Re yang mahal dan langka.

“Kami berusaha untuk menggunakan larutan yang ramah lingkungan. Rute transformasi kimia (sintesis organik) secara fotokatalisis (misalnya menggunakandengan Cu(I)Ox-C3N4 ) sangat menjanjikan karena kita hanya menggunakan katalis, cahaya, dan air (sebagai pelarut). Katalisnya juga murah, kemudian cahaya ada di mana-mana. Salah satu tantangan terbesar adalah bagaimana menemukan cara yang efisien dan murah untuk konversi temuan di skala lab ke skala industri, pungkas tim kelompok riset perangkat dan teknologi kuantum. (hrd/ ed: adl)